tất cả những bí quyết hóa học tập lớp 8
I. CÔNG THỨC TÍNH SỐ MOL (MOL)1. Theo khối lượng:n = m/MTrong đó:m: khối lượngM: cân nặng phân tử, trọng lượng mol
Ví dụ 1Cho 2,4 gam Mg vào hỗn hợp HCl dư. Tính thể tích khí hiđrô thu được làm việc điều kiệnchuẩn. (Cho Mg=24)2. Theo thể tích (đối với hóa học khí ở điều kiện chuẩn) :n =V/22,4Trong đó:V: thể tích khí
Ví dụ 2Cho 6,75 gam sắt kẽm kim loại nhôm vào dung dịch H2SO4 loãng . Phản nghịch ứng kết thúc thu được3,36 lít khí (đktc).a. Viết phương trình làm phản ứng.b. Tính cân nặng muối nhận được sau làm phản ứng.(Cho: Zn = 65; H = 1; S = 32; O = 16)II. CÔNG THỨC TÍNH NỒNG ĐỘ DUNG DỊCH
1. Nồng độ mol /lít (CM)CM =n/V (M)

Ví dụ 3
Để trung hoà hết 200 gam hỗn hợp Na
OH 10% buộc phải dùng bao nhiêu gam hỗn hợp HCl 3,65%.
Bạn đang xem: Tất cả những công thức hóa học lớp 8
(cho mãng cầu = 23; Cl = 35,5; O = 16; H = 1)
Ví dụ 4
Cho 200ml dung dịch Na
OH 8% tất cả D = 1,15g/ml tác dụng với 380 gam dung dịch Mg
Cl25%.
Thế là hoàn thành nhé các bạn
Các công thức được chụp bởi hình là
Công thức liện hệ C%, CM, cân nặng riêng D
Công thức tính cân nặng riêng (D)
Nồng độ phần trăm
Công thức tính thành phần phần trăm
Phần trăm theo khối lượng:Phần trăm theo cầm tích (chính là tỷ lệ theo số mol):Các phương pháp hóa học tập lớp 8, 9 cơ phiên bản cần nhớ
Các phương pháp hóa học lớp 8 cơ phiên bản cần nhớ bao gồm có: công thức tính số Mol, phương pháp tính nồng độ Mol, cách làm tính độ đậm đặc %, công thức tính khối lượng, phương pháp tính thể tích dung dịch…
21 cách làm hóa học tập lớp 8, 9 đề nghị nhớ


⚗️ GIA SƯ HÓA
Tổng hợp những công thức hóa học lớp 8 phải nhớ – chăm đề 1
Môn chất hóa học lớp 8 giới thiệu đến những em những kiến thức và kỹ năng căn bạn dạng nhất của môn Hóa học. Nắm nào là chất, cố gắng nào là nguyên tố hóa học. Nguyên tử với phân tử khác biệt ở đâu. Tuy nhiên song cùng với đó, những em cũng trở thành được học một vài công thức hóa học.
Dưới đấy là tổng hợp những công thức hóa học lớp 8 cần nhớ trực thuộc chương lắp thêm nhất: chất – Nguyên tử – Phân tử – Hóa trị. Ví dụ là những công thức liên quan đến khối lượng nguyên tử, trọng lượng phân tử, quy tắc hóa trị của một chất.
1, Tổng hợp các các cách làm hóa học lớp 8 cần nhớ – Phần 1: chất – Nguyên tửKiến thức trung tâm về Chất
Chất có ở mọi nơi, nơi đâu có đồ vật thể, ngơi nghỉ đó tất cả chất.
Vật thể bởi một chất hoặc nhiều chất sản xuất nên. Ví như ấm nhôm vị nhôm chế tác nên, xe đạp điện do các chất sắt, nhôm, cao su tạo nên.
Mỗi một chất lại có những tính chất vật lí và tính chất hóa học nhất định. Ví như nước sôi nghỉ ngơi 100 độ C với đông đặc ở 0 độ C. Đường gồm vị ngọt, đồng gồm màu đỏ
Hỗn hợp: nhị hay nhiều chất trộn lẫn vào cùng nhau thì gọi là lếu láo hợp. Chăm chú rằng, nước tự nhiên gồm nhiều chất trộn lẫn là 1 trong những hỗn hợp. Còn nước đựng là hóa học tinh khiết
Tách chất ra khỏi hỗn hợp: nhờ vào sự không giống nhau về đặc điểm vật lý như tính tan, nhiệt độ sôi của các chất tất cả thể tách bóc được một chất thoát ra khỏi hỗn hợp
Kiến thức trung tâm về Nguyên tử
Nguyên từ bỏ được quan niệm là phân tử vô cùng bé dại và th-nc về điện.
Cấu tạo thành của nguyên tử gồm gồm vỏ nguyên tử và hạt nhân nguyên tử
Hạt nhân nguyên tử gồm có 3 một số loại hạt là hạt proton có điện tích dương, hạt notron không mang điện với hạt electron có điện tích âm.
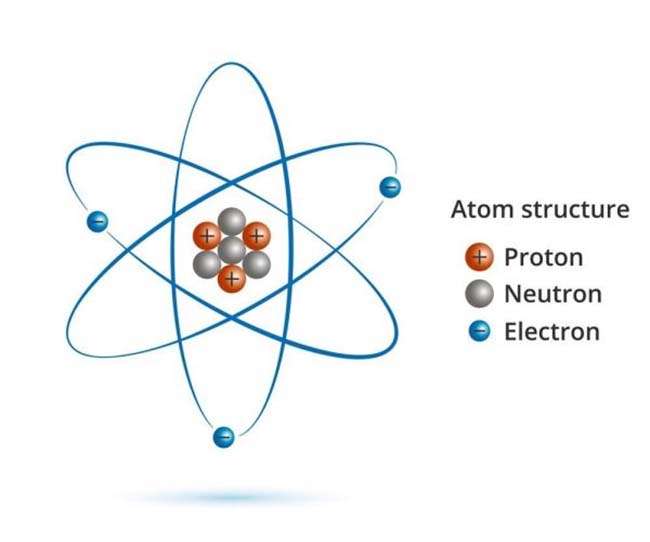
Đặc điểm và phương pháp hạt nhân nguyên tử
Nguyên tử trung hòa về điện đề xuất số proton ngay số electron. Ta tất cả công thứcp = e.Đây là một trongcác cách làm hóa học tập cơ bạn dạng thcsElectron luôn chuyển động quanh hạt nhân và sắp xếp thành từng lớpProton và notron gồm cùng khối lượng. Ta bao gồm công thức: m (p) = m (n)electron có khối lượng rất bé bỏng không đáng kể, nên cân nặng hạt nhân cũng là khối lượng hạt nhân. Ta gồm công thức: m (nguyên tử) = m (hạt nhân)
Kiến thức trung tâm về yếu tắc hóa học
Nguyên tố hóa học: Là tập hợp đầy đủ nguyên tử cùng loại,có cùng số proton trong phân tử nhân. Mỗi nguyên tố chất hóa học lại được màn biểu diễn bằng một kí hiệu hóa học. Ví dụ: Na, K, S, Cl, Fe
Nguyên tử khối là cân nặng của một nguyên tử tính bằng đơn vị cacbon. Từng nguyên tử gồm một trọng lượng riêng biệt,
Đơn vị cacbon (đv
C): 1 đv
C = 1/12 m (Cacbon)
Trong đó cân nặng nguyên tử C – m (Cacbon) = 1, 9926. 10-23
2, Tổng hợp những các phương pháp hóa học tập lớp 8 đề xuất nhớ – Phần 2: Phân tử
Phân tử là thay mặt cho chất, gồm một vài nguyên tử liên kết với nhau cùng thể hiện đầy đủ tính hóa chất của chất
Phân tử bao gồm hai dạng là đối chọi chất cùng hợp chất
Đơn chất: là đông đảo chất khiến cho từ một yếu tắc hóa học. Khí Hidro (H2) là 1-1 chất, được làm cho từ 1 nguyên tố hóa học là hidro. Trong đối kháng chất lại được chia thành 2 một số loại là đối chọi chất kim loại và solo chất phi kim. Đơn chất kim loại có tính dẻo, tính dẫn điện, tính dẫn nhiệt, ánh kim,…Hợp chất: là rất nhiều chất làm cho từ nhì nguyên tố hóa học trở lên. NaCl là vừa lòng chất, được làm cho từ 2 nhân tố hóa học chính là natri (Na) cùng clo (Cl)
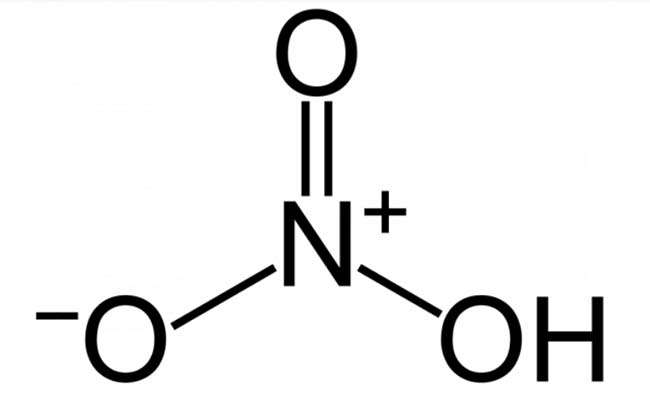
công thức hóa học đầy đủtính cân nặng phân tử:
Phân tử khối = khối lượng phân tử (đv
C) = tổng cộng nguyên tử thành phần . Nguyên tử khối
Ví dụ đối kháng chất: Phân tử ni tơ bao gồm 2 nguyên tử N. Vậy phân tử khối của ni tơ được tính bằng 2 lần nguyên tử khối của nguyên tử N và bằng 2.14 = 28 (đv
C)
Ví dụ hợp chất: Một phân tử axit clohidric (HCl) được cấu tạo từ 1 nguyên tử Hidro (H) với một nguyên tử Clo (Cl). Vậy phân tử khối của axit clohidric được tính bằng tổng của nguyên tử khối của H và Cl và bằng 1 + 35,5 = 36,5 (đv
C)
Công thức chất hóa học của đơn chất được kí hiệu dưới 2 dạng là A với Ax
Trong kia A thường xuyên là solo chất sắt kẽm kim loại với một vài ba phi kim, lấy một ví dụ Na, Fe, Cu, P, C, SCòn Axthường là đối kháng chất phi kim, tất cả 2 nguyên tử link với nhau: O2, H2, N2Công thức hóa học của hợp chất gồm công thức Ax
By
Cz
Trong đó A, B, C là những kí hiệu hóa học còn x, y, z là những chỉ số chân, cho thấy số nguyên tử của nguyên tố gồm trong một phân tử
Ý nghĩa của công thức hóa học: phương pháp hóa học của mỗi chất cho biết
Số nguyên tố tạo thành chấtSố nguyên tử của mỗi nguyên tố
Phân tử khối
Ví dụ: axit sunfuric gồm công thức hóa học là H2SO4
Vậy axit sunfuric vì 3 nguyên tố H, S, O tạo ra ra
Trong 1 phân tử axit sunfuric có 2 nguyên tử H, 1 nguyên tử S cùng 4 nguyên tử O
Phân tử khối của một phân tử axit sunfuric bằng 2.1 + 1.32 + 4.16 = 98 (đv
C)
Hóa trị của một nhân tố (hay một đội nhóm nguyên tử) là nhỏ số biểu lộ khả năng liên kết của nguyên tử (hay team nguyên tử), được xác định theo
Hóa trị của H, hóa trị của H được chọn làm đơn vị, hóa trị của H là một đơn vị
Hóa trị của O là 2 đối kháng vị
Quy tắc hóa trị: Ax
By-> a.x = b.y
Đây là phương pháp hóa trị cơ bản nhất, từ bí quyết này, ta cócác công thức hóa học lớp 9liên quan mang đến hóa trị sau này
Trong đó
a, b là hóa trị của nguyên tố.
x, y là chỉ số tuyệt số nguyên tử của nguyên tố
5, bài bác tập vận dụng một số trong những các công thức hóa học tập lớp 8 đề nghị nhớBài tập 1: Tổng số hạt proton, notron, electron vào nguyên tử là 28 hạt, trong đó số phân tử không với điện là 10. Tính số hạt mỗi loại
Hướng dẫn giải
Hạt không sở hữu điện là notron, vậy n = 10
Tổng số phân tử proton, notron với electron vào nguyên tử là 28 buộc phải ta áp dụngcác công thức hóa học tập lớp 8 buộc phải nhớcó phường + n + e = 28 (1)
Vì số proton bằng số electron phải từ (1) ta gồm 2p + n = 28, mà n = 10 buộc phải ta gồm số p. = số e = 9
Vậy ta tất cả số hạt proton và electron là 9, số notron là 10
Bài tập 2: a) Tính phân tử khối của mỗi chất sau: axit nitric, can xi sunfat, sắt III oxit, bari hidroxit
b) xác định % khối lượng của oxi trong mỗi phân tử trênHướng dẫn giải
a) axit nitric: HNO3có phân tử khối là M = 1 + 14 + 3.16 = 63 (đvC)
canxi sunfat: Ca
SO4có phân tử khối là M = 40 + 32 + 4.16 = 120 (đv
C)
sắt III oxit: Fe2O3có phân tử khối là M = 56.2 + 16.3 = 160 (đv
C)
bari hidroxit Ba(OH)2có phân tử khối là M = 137 + 2.(16+1) = 171 (đv
C)
% Oxi trong canxi sunfat là: 4.16 / 120 = 53,33%
% Oxi trong sắt III oxit là: 16.3 / 160 = 30%
% Oxi trong bari hidroxit: 32 / 171 = 18,71%
Trên đây là toàn bộcác bí quyết hóa học tập lớp 8 yêu cầu nhớliên quan mang đến chương trước tiên của hóa học lớp 8: hóa học – Nguyên tử – Phân tử – Hóa trị. Để có thể làm được những bài tập của phần này, các em học sinh cần ráng được những bí quyết tổng hợp trong bài cũng tương tự xem kĩ lại các bài tập ví dụ đã có giải chi tiết phía trên.
Công thức chất hóa học | bài tập lập phương pháp hóa học trường hợp biết hóa trị
Lập công thức Hóa học là một trong không ít dạng bài cơ phiên bản khi học tập môn hóa học lớp 8 được đặt theo hướng dẫn giải đầy đủ. Họ cần nắm được cách làm cùng một số để ý rất đặc biệt quan trọng thì lập công thức hóa học tập nhanh, đúng mực rất các
1. Lập bí quyết của 1-1 chất
Lập cách làm hóa học tập của Kim loạiCông thức chất hóa học được tạo thành các các loại như phương pháp hóa học của sắt kẽm kim loại thường trùng với cam kết hiệu chất hóa học của kim loại đó
Ví dụ:Công thức chất hóa học của Natrium là Na
Công thức hóa học của Kalium là KCông thức chất hóa học của Canxium là Ca
Công thức chất hóa học của fe là sắt
Công thức chất hóa học của phi kim hay tồn tại sinh sống dạng khí nên những lúc thể hiện tại trên phương pháp hóa học chúng ta thường có hai nguyên tử của yếu tố phi kim link với nhau
Ví dụ:Công thức chất hóa học của Hidro là H2Công máy hóa học tập của Clo là Cl2Công thức chất hóa học của Nitơ là N2Công thức chất hóa học của Oxy là O2Một số quy ước khác, bí quyết hóa học phi kim cũng hoàn toàn có thể là cam kết hiệu hóa học
Ví dụ:Công thức hóa học của Cácbon là CCông thức hóa học của Phốt pho là PCông thức hóa học của đúng theo chất
Công thức hóa học của sulfur là S
2. Lập cách làm của thích hợp chất
Hợp chất hóa học là các thành phần hỗn hợp được khiến cho bởi nhị hoặc những nguyên tố chất hóa học khác nhau.Khi bọn họ lập bí quyết của hợp chất hóa học họ cần phải nắm vững được quy tắc hóa trị.Hóa trị là gì?Hóa trị làcủa một nguyên tố được khẳng định bằng số links hóa học mà lại một nguyên tử của nguyên tố đó làm cho trong phân tử
Quy tắc hóa trị là gì ?Xét một hợp chất hóa học tất cả công thức bao quát

3. Bài bác tập lập cách làm Hóa Học
Bài 1: Lập công thức Hóa Học của các hợp hóa học sau đây:a. Lập cách làm hóa học của Cu(II) với Clo tạo ra thành hợp hóa học Đồng Clorua

Theo phép tắc hóa trị ta có: 2x=y
Chọn x=1, y=2 ta được công thức hóa học tập của đồng clorua là

b. Lập cách làm hóa học thân Al với (NO3) sinh sản thành chất Nhôm Nitơrát

– Theo quy tác hóa trị ta có: 3x=y
Chọn x=1, y=3 ta được bí quyết hóa học của Nhôm Nitơrát là

c.Lập bí quyết hóa học của can xi Phốt phát đựng nguyên tố Ca cùng nhóm phốt phạt (PO4) gồm số hóa trị là 3Bài giải:– Gọi bí quyết hóa học tập của hợp hóa học là

– Theo nguyên tắc hóa trị ta có: 2x=3y
Chọn x=3, y=2 ta được phương pháp Hóa học của can xi photphat là

Bài 2: Lập cách làm hóa học tập của sắt bao gồm hóa trị khớp ứng trong bí quyết Fe
Cl2 với team (OH) bao gồm hóa trị I.
Bài viết nghĩ rằng là một trong những kiến thức khá thú vị về tất cả những công thức hóa học lớp 8, ko phải là một trong những kiến thức làm sao xa lạ, nhưng nói theo cách khác môn hóa là một trong bộ môn nó dính liền cùng với nhau, kỹ năng và kiến thức lớp new nó có tương quan tới kiến thức và kỹ năng lớp cũ. Vị vậy các công thức của lớp cũ ko nhớ sẽ gặp gỡ khó khăn trong câu hỏi giải bài bác tập môn hóa học. Bài này gia sư trí óc Việt phân tách sẽ bài viết các công thức hóa học thường gặp, phần nhiều năm trong lịch trình lớp 8 và lớp 9, họ cùng ban đầu nào.
Contents
2 II. CÔNG THỨC TÍNH NỒNG ĐỘ DUNG DỊCHI. CÔNG THỨC TÍNH SỐ MOL (MOL)
1. Theo khối lượng: n = m/M trong đó: m: trọng lượng M: khối lượng phân tử, cân nặng mol
ví dụ như 1 cho 2,4 gam Mg vào hỗn hợp HCl dư. Tính thể tích khí hiđrô nhận được ở điều kiện chuẩn. (Cho Mg=24) 2. Theo thể tích (đối với chất khí ở điều kiện chuẩn) : n =V/22,4 vào đó: V: thể tích khí ví dụ 2 mang đến 6,75 gam kim loại nhôm vào hỗn hợp H2SO4 loãng . Phản ứng kết thúc thu được 3,36 lít khí (đktc). A. Viết phương trình bội phản ứng. B. Tính khối lượng muối nhận được sau phản ứng. (Cho: Zn = 65; H = 1; S = 32; O = 16)
II. CÔNG THỨC TÍNH NỒNG ĐỘ DUNG DỊCH
1. Mật độ mol /lít (CM) centimet =n/V (M)
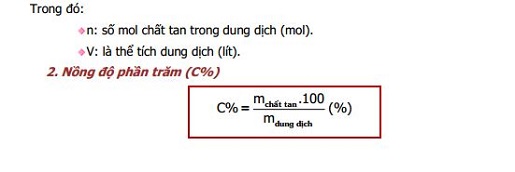
Ví dụ 3
Để trung hoà không còn 200 gam hỗn hợp Na
OH 10% buộc phải dùng bao nhiêu gam dung dịch HCl 3,65%.
(cho na = 23; Cl = 35,5; O = 16; H = 1)
Ví dụ 4
Cho 200ml dung dịch Na
OH 8% gồm D = 1,15g/ml công dụng với 380 gam hỗn hợp Mg
Cl2 5%.
Xem thêm: Bảng ký tự đặc biệt cf, game đột kí tự đặc biệt cf người chơi không nên bỏ qua
Thế là kết thúc nhé những bạn
Các cách làm được chụp bằng hình là
Công thức liện hệ C%, centimet , cân nặng riêng D
Công thức tính cân nặng riêng (D)
Nồng độ phần trăm
Công thức tính nhân tố phần trăm
Phần trăm theo khối lượng:Phần trăm theo vắt tích (chính là phần trăm theo số mol):Trên tất cả những cách làm hóa học thường xuyên xuyên gặp gỡ nhất trong quy trình giải bài bác tập, mong muốn rằng chúng ta có được chút kiến thức và kỹ năng từ bài viết của Trung trung khu Gia Sư day kem TTV bọn chúng tôi