Để giúp các em học sinh có ánh nhìn tổng quan về ngôn từ Chương 4 chất hóa học 9, HOC247 đã biên soạn và tổng phù hợp tài liệu
Ôn tập Hóa 9 Chương 4. Đây là những kỹ năng căn bạn dạng trọng trung ương làm nền tảng gốc rễ xuyên suốt mang lại chương trình hóa học THPT. Vày vậy những em đề xuất ghi ghi nhớ được những khái niệm, các công thức hóa học để áp dụng sau này. Trong tư liệu này còn cung cấp thêm nội dung những bài học, giải bài tập SGK và kèm theo những bài tập trắc nghiệm có không thiếu thốn đáp án, lời giải chi tiết nhằm giúp những em ôn tập và củng cố kiến thức và kỹ năng một cách hiệu quả. Mong muốn đây vẫn là tư liệu hữu ích cho các em trong việc học tập. Chúc các em ôn tập tốt, đạt hiệu quả cao!
YOMEDIA
Đề cưng cửng ôn tập hóa học 9 Chương 4
A. Bắt tắt lý thuyết
1. Khối hệ thống kiến thức về Hiđrocacbon| Metan | Etilen | Axetilen | Benzen | |
Công thứccấu tạo | 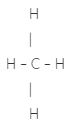 | H2C = CH2 | HC CH | 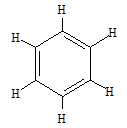 |
Đặc điểmcấu tạo củaphân tử | Chỉ có links đơn. Bạn đang xem: Giải bài tập hóa 9 chương 4 | Có một links đôi, bao gồm 1 liên kết bền với 1 links yếu | Có một liên kết ba, bao gồm một liên kết bền với 2 link yếu. | Mạch vòng, bao gồm 3 links đôi xen kẽ 3 link đơn |
Phản ứngđặc trưng | Phản ứng thế | Phản ứng cộng. | Phản ứng cộng 2 nấc | Vừa tất cả phản ứng cầm vừa gồm phản ứng cộng |
| Ứng dụng chính | Nhiên liệu | Nguyên liệu cấp dưỡng chất dẻo, rợu etylic... | Nguyên liệu tiếp tế chất dẻo, axit axetic, đèn xì oxi - axetilen... | Nguyên liệu chế tạo chất dẻo, phẩm nhuộm, dung dịch trừ sâu, dung môi trong công nghiệp... |
2. Sơ đồ tư duy tổng kết bài xích học
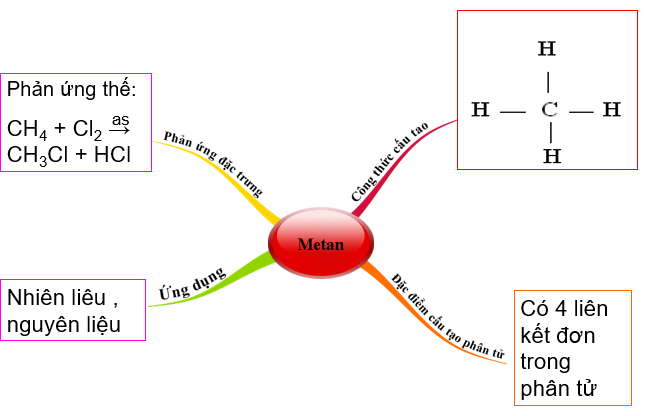
Hình 1:Sơ đồ tứ duy về Metan
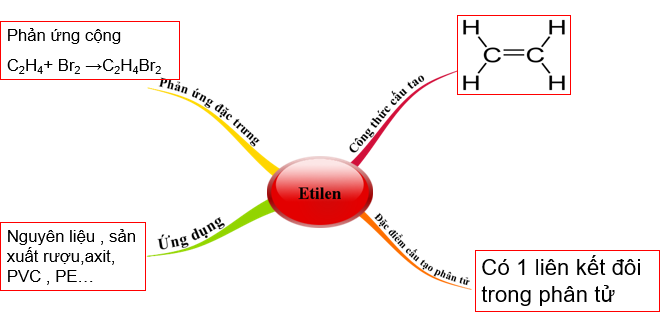
Hình 2:Sơ đồ tư duy về Etilen
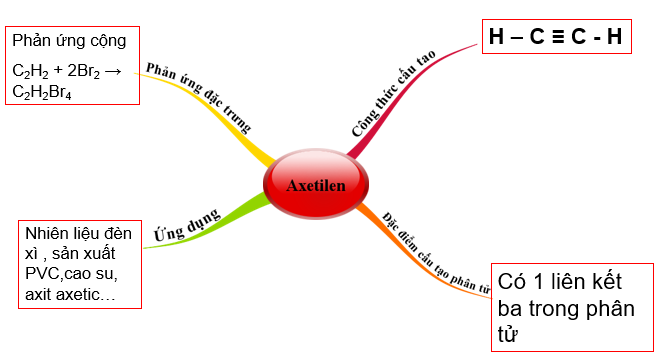
Hình 3:Sơ đồ tư duy về Axetilen
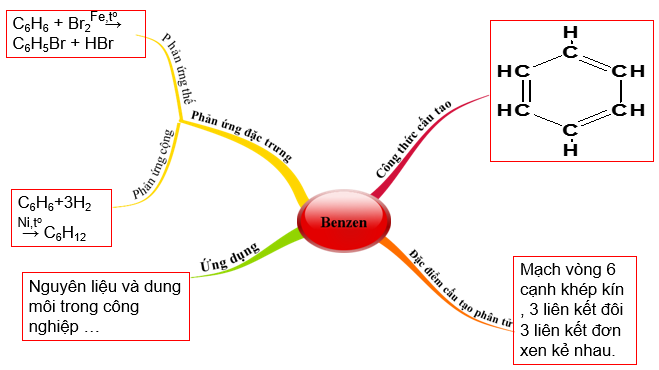
Hình 4:Sơ đồ bốn duy về Benzen
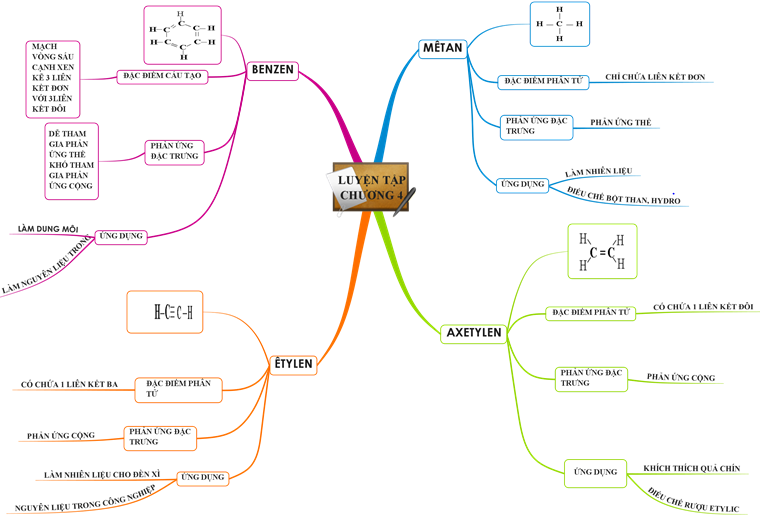
Hình 5:Sơ đồ tứ duy về Hidrocacbon
B. Bài bác tập minh họa
Bài 1:Có 3 bình không nhãn đựng những khí sau: CH4, CO2, C2H4. Bằng phương thức hóa học, hãy nhận thấy chúng.
Hướng dẫn:Dùng dd Brom phân biệt C2H2:C2H2 + Br2 → C2H4Br2
Dùng nước vôi trong nhận biết CO2, khí còn sót lại là CH4: CO2 + Ca(OH)2 → Ca
CO3 + H2O
Đốt cháy hoàn toàn 6,72 lit khí C2H2.
a, Viết phương trình phản bội ứng xảy ra?
b, Tính trọng lượng CO2thu được.
c, Cho toàn bộ lượng CO2thu được trải qua dung dịch Ca(OH)2dư. Tính cân nặng chất rắn thu được?
Hướng dẫn:a. Số mol khí C2H2tham gia phản ứng là:
Phương trình bội nghịch ứng: 2C2H2 + 5O2
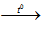
Số mol theo phương trình: 2 mol 5 mol 4 mol 2 mol
Số mol theo đề bài: 0,3 mol → 0,6 mol
b.Khối lượng CO2thu được là:
m CO2= n.M = 0,6. 44 = 24,4 g
c.Khi cho CO2đi qua hỗn hợp Ca(OH)2; phương trình phản ứng xảy ra là:
CO2 + Ca(OH)2 → Ca
CO3 + H2O
Từ phương trình ta bao gồm n
Ca
CO3 = 0,6 mol
Khối lượng hóa học rắn Ca
CO3thu được là: 0,6.100 = 60 gam
Trắc nghiệm hóa học 9 Chương 4
Đề khám nghiệm Hóa học 9 Chương 4
Trắc nghiệm online hóa học 9 Chương 4 (Thi Online)Phần này các em được gia công trắc nghiệm online cùng với các câu hỏi để kiểm tra năng lực và sau đó đối chiếu hiệu quả từng câu hỏi.
Đề soát sổ Hóa học tập 9 Chương 4 (Tải File)Phần này các em hoàn toàn có thể xem online hoặc cài file đề thi về xem thêm gồm đầy đủ thắc mắc và đáp án làm bài.
Lý thuyết từng bài xích chương4 và trả lời giải bài xích tập SGK
Lý thuyết chất hóa học 9 Chương 4Giải bài xích tập hóa học 9 Chương 4Trên đây là nội dung đề cương ôn tập Hóa 9 Chương 4. Hi vọng với tài liệu này, những em để giúp các em ôn tập và khối hệ thống lại kỹ năng thật tốt. Để thi online và sở hữu file đề thi về máy những em vui miệng đăng nhập vào trang hoc247.netvà ấn chọn tác dụng "Thi Online" hoặc "Tải về".Ngoài ra, các em còn có thể share lên Facebook nhằm giới thiệu bạn bè cùng vào học, tích lũy thêm điểm HP với có thời cơ nhận thêm nhiều phần quà có mức giá trị trường đoản cú HỌC247 !
Để củng ráng lại kỹ năng và kiến thức về chương 4. docongtuong.edu.vn xin chia sẻ với các bạn bài: rèn luyện chương 4: Hiđrocacbon - Nhiên liệu. Với kiến thức trọng trung khu và các bài tập có giải mã chi tiết, hi vọng rằng đây đã là tư liệu giúp chúng ta học tập tốt hơn.

Ôn tập lý thuyếtHướng dẫn giải bài tập sgk
A. LÝ THUYẾT
I. METAN
1. Cấu tạo phân tửCTCT của metan (CH4)
2. đặc thù hóa học
Tác dụng với oxi:CH4+ 2O2→ CO2+ 2H2O
Tác dụng cùng với clo khi bao gồm ánh sáng:(phản ứng thế)CH4+ Cl2→HCl + CH3Cl
3. Ứng dụng
Dùng làm cho nhiên liệu.II. ETILEN
1. Bí quyết cấu tạo
Etilen tất cả công thức cấu tạo:
2. đặc điểm hóa học
Tác dụng cùng với oxi:.
C2H4+ 3O2→(to) 2CO2+ 2H2O
Tác dụng với dung dịch brom:phản ứng cộng
CH2=CH2+ Br2→ Br – CH2– CH2– Br
Phản ứng trùng hợp
…+ CH2=CH2+ CH2=CH2+ CH2=CH2+ … →(to, xt, p) …CH2– CH2– CH2– CH2– CH2– CH2…
3. Ứng dụng
Etilen dùng làm sản xuất axit axetic, rượu etylic, poli (vinyl clorua),...Etilen dùng kích mê thích quả mau chín.III. AXETILEN
1. Cấu tạo phân tử
Axetilen tất cả một links ba thân hai nguyên tử cacbon.Công thức cấu trúc của axetilenH – C ≡ C – H;Viết gọnHC ≡ CH.2. đặc thù hóa học
Tác dụng cùng với oxi:
2C2H2+ 5O2→(to) 4CO2+ 2H2O
Tác dụng với hỗn hợp brom:
HC=CH + Br2→ Br – CH=CH – Br
HC=CH + Br2→ Br2CH – CHBr2
Trong đk thích hợp, axetilen còn tham gia phản ứng cộng với nhiều chất khác ví như H2, Cl2...
3. Ứng dụng
Axetilen cần sử dụng trong đèn xì oxi-axetilen dể hàn, giảm kim loại.Axetilen là nguyên vật liệu để tiếp tế poli (vinyl clorua) cần sử dụng sản xuất nhựa PVC và những hóa hóa học khác.Xem thêm: Cách đặt biệt danh cho bạn bè trên facebook không đụng hàng, đặt biệt danh trong facebook messenger thế nào
IV. BENZEN
1.Cấu sản xuất phân tử
6 nguyên tử C link với nhau chế tác thành vòng, 3 link đôi xen kẹt 3 links đơn
2. đặc điểm hóa học
Phản ứng cháy:
2C6H6+ 15O2→(to)12CO2+ 6H2O
Phản ứng thay với cùng với brom:
C6H6(l) + Br2(l) →HBr + C6H5Br (brom bezen)
Phản ứng cộng:
C6H6+ 3H2→(to, Ni)C6H12
3. Ứng dụng
Benzen là nguyên liệu đặc biệt quan trọng để tiếp tế chất dẻo, phẩm nhuộm, dược phẩm, dung dịch trừ sâu.. Benzen làm cho dung môi, hòa tan những chất hữu cơ.